17β-雌二醇( 17β-Estradiol,E2) 是常见的内分泌干扰物之一,环境中存在的 E2 可直接或间接进入 生物体,具有致癌致畸效应. 因此,开发简单、灵敏和高选择性的 E2 检测技术十分必要. 传统的 E2 检测方法有高效液相色谱法、气相色谱-质谱联用技术、酶联免疫技术和电化学方法等. 这些检测方法或需要精密仪器,或检测步骤繁琐,而且电化学方法直接测定 E2 的灵敏度和选择性还 有待提高.
1 实验部分
1.1 试剂与仪器
17β-雌二醇( E2) 、雌三醇( E3) 、双酚 A( BPA) 和对苯二酚( HQ) 均为分析纯,购于北京百灵威科技有限公司; 氯金酸( HAuCl4·4H2O,分析纯) 和硫堇( THI,分析纯) 购于国药集团化学试剂有限公 司; 纳米二硫化钼分散液( MoS2,分析纯) 购于南京牧科纳米科技有限公司; 17β-雌二醇适配体 ( 17β-Estradiol aptamer DNA) 和部分互补单链 DNA( cDNA) 经高效液相色谱( HPLC) 纯化,由生工生物 工程( 上海) 股份有限公司合成,其碱基序列分别为 Aptamer DNA 5'-SH-( CH2 ) 6-GCT TCC AGC TTA TTG AAT TAC ACG CAG AGG GTA GCG GCT CTG CGC ATT CAA TTG CTG CGC GCT GAA GCG CGG AAG C 和 cDNA 5'-SH-( CH2 ) 6-TTT GAG CTT CCG CGC TTC AGC GCG CAG CAA; 实验用水为超纯水. CHI660E 型电化学工作站( 上海辰华仪器公司) ,实验采用三电极系统: 二硫化钼/纳米金修饰玻 碳电极( GNPs-MoS2 /GCE) 为工作电极,饱和甘汞电极( SCE) 为参比电极,铂片电极为对电极; SU8220 型场发射扫描电子显微镜( SEM,日本 Hitachi 公司) ; UV-2550 型紫外-可见分光光度计( 日本岛津公 司) ; 昆山舒美KQ-100DB 超声波清洗机( 江苏昆山超声仪器公司) .
1.2 电化学适配体传感器的制备及测定
参考方法合成纳米金溶胶( GNPs) ,用紫外-可见分光光度计表征 GNPs 的特征吸收峰为 519 nm. 参照方法进行玻碳电极( GCE) 的预处理. 电化学适配体传感器的制备及原理如 Scheme 1所示. 参照方法制备 GNPs-MoS2 修饰电极: 将 1 mg /mL MoS2 溶液超声分散 2 h,取 5 μL滴涂于预处理好的 GCE 表面,室温下自然晾干. 将 MoS2 修饰电极置于含 6 mmol /L 氯金酸的 0. 1 mol /L KCl 溶液中,在-0. 2 V( vs. SCE) 恒电位条件下沉积 80 s,即得到 GNPs-MoS2 修饰电极. 将 5 μL 1. 0×10-6 mol /L 适配体 DNA 滴涂到修饰电极表面,于 4 ℃ 冰箱中放置 12 h,分别用超纯水和 0. 01 mol /L Tris-HCl( pH = 7. 4) 缓冲溶液冲洗吸附的适配体 DNA. 为了防止非特异性吸附,将电极浸泡 于1 mg /mL的牛血清白蛋白( BSA) 溶液中,于 38 ℃放置 1 h 后,用超纯水和 0. 01 mol /L Tris-HCl 缓冲 溶液( pH = 7. 4) 冲洗表面,再与 1. 0×10-6 mol /L 部分互补 cDNA 于 38 ℃杂交反应 70 min. 在杂交后的 电极表面滴加 9 μL 合成的 GNPs,室温下避光静置 4 h; 再置于 0. 25 mmol /L 的 THI 溶液中避光静置 50 min后,用超纯水和 0. 01 mol /L Tris-HCl 缓冲溶液( pH = 7. 4) 冲洗以除去未吸附的 GNPs 和 THI,获 得适配 体 传 感 器 ( THI-GNPs / dsDNA /BSA / ssDNA /GNPs-MoS2 /GCE) . 在 5 mmol /L K3[Fe ( CN) 6]/ 5 mmol /L K4[Fe( CN) 6]/10 mmol /L KCl 溶液中,采用循环伏安( CV) 法和电化学交流阻抗( EIS) 法对 传感器进行表征.
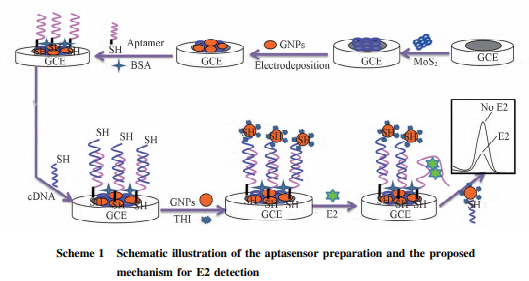
室温下,将制备的传感器置于不同浓度的 E2 溶液中反应 50 min,反应结束后用超纯水和 0. 01 mol /L Tris-HCl 缓冲溶液( pH = 7. 4) 冲洗电极表面,然后置于 0. 01 mol /L Tris-HCl 缓冲溶液( pH = 7. 4) 中,采用差分脉冲伏安( DPV) 法对 E2 进行定量测定,记录 THI 的氧化峰电流,用反应前后目标物 E2 的 ΔI[ΔI = I0-I) [其中,I0( μA) 为反应初始电流; I( μA) 为反应后的电流,ΔI( μA) 为反应前后的电流 变化]进行定量分析.
2 结果与讨论
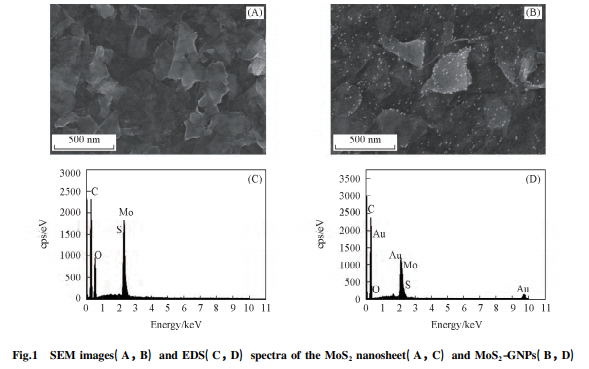
图 1 为 MoS2 /GCE 和 GNPs-MoS2 /GCE 的 SEM 照片和能谱分析( EDS) 图. 由图 1( A) 可知,纳米 MoS2 呈层状薄片分布,片层之间有孔道. 由图 1( B) 可见,20 ~ 30 nm 的颗粒物分布在 MoS2 层状薄片 上,表明 GNPs 已制备. 在图 1( C) 中可以观察到 Mo,S,C 和 O 的峰,在图 1( D) 可以观察到 Au,Mo, S,C 和 O 的峰,其中 C 和 O 为 GCE 电极的基体元素,Mo 和 S 峰为 MoS2 的峰. 而 Au 峰的存在进一步 证明 MoS2 表面分布的颗粒物为 GNPs.
THI 具有良好的电化学氧化还原可逆性和稳定性,近年来被作为电化学免疫传感器和电化学 DNA 传感器的电化学指示剂. GNPs 作为信号物质载体,可与 THI 分子形成金-硫、金-氮键合作用及 Fig.3 CV response of the electrochemical aptasensor interacted with different concentrations of E2 in 0. 01 mol /L Tris-HCl solution ( pH= 7. 4) cE2 /( mol·L-1 ) : a. 0; b. 1. 0×10-13 ; c. 1. 0×10-12 . 静电吸附作用,从而制备 GNPs /THI 电化学指示 剂; GNPs 的大比表面积为 THI 提供了大量结合位 点,可实现电化学信号的放大.
3 结 论
基于双信号放大建立了电化学适配体传感器检测 E2 的分析方法. 实验结果表明,该方法检测 E2 的检出限为 4. 2×10-15 mol /L( S /N= 3) . 该方法检出限较低、线性范围较宽、特异性较好,可用于环境 水样中 E2 的检测,并有望用于其它环境样品中 E2 的测定.
免责声明:文章仅供学习和交流,如涉及作品版权问题需要我方删除,请联系我们,我们会在第一时间进行处理。